生物安全第三等級實驗室 Biosafety Level 3 Lab
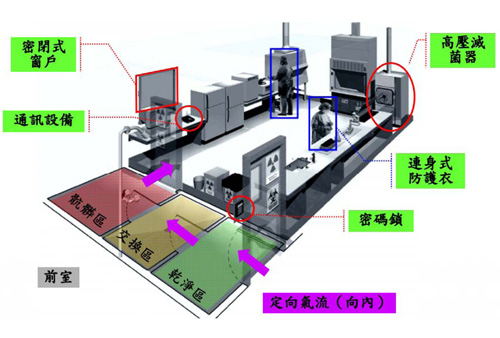
1.適用範圍
BSL-3 實驗室適用於處理第三級危險群微生物及大量或高濃度、具有高度氣膠擴散危險之第二級危險群微生物之工作。
2.實驗室設施規範
A.實驗室位置
在一棟建築物裏,BSL-3 實驗室與其他設施之相對位置係實驗室管制之重要因子。BSL-3 實驗室位置安排適當可使人員進出易於管制,且亦能整合低管制區與高管制區,集中管理必要之勤務支援系統(如消毒、廢棄物處理與空調處理系統等)。
a.實驗室與公共區域應明確分開及識別,可以門做清楚的區隔,惟應符合其他相關法規之規定
b.實驗室應為密閉空間,具通道管制的獨立且專用的進排氣系統。進排氣系統之維護路徑與實驗室操作人員工作路徑應明確區隔。
c.由公共通道進入實驗室阻隔區(containmentarea)之路徑,應以實施管制之前室(anteroom)予以區隔。
B. 實驗室隔間牆之物理結構
實驗室隔間牆係提供物理性隔絕功能,其表面應易於清潔與殺菌處理。因此,選擇實驗室牆板材質與填縫劑時,必須考慮抗化學性、耐久性、不透水氣,以及與其他建材的相容性; 在設計與施工時,須考慮到實驗室長期使用與未來發展。
此外,實驗室需要負壓區,實驗室之密閉結構須能抵禦不可避免之氣壓衝擊(例如門啟閉瞬間之氣壓變化、室內生物安全櫃等抽氣設備啟閉瞬間之氣壓變化等),故在設計牆板與天花板時亦須有負壓考量。
a.隔間牆之施工須採無縫工法,或其他足以長時間維持隔間牆氣密狀態之工法。
b.若因故(穿牆管路、穿牆電氣線路等)必須於隔間牆、天花板鑽孔施工時,施工後應將遺留的孔隙以耐酸鹼、耐衝擊之材料填縫密封,以確保實驗室之氣密。
c.在實驗室周界內所有氣體供應管路之貫穿孔,必須以非壓縮性填充物密封。天花板得以暗架施工,但應以氣密處理。如有保留檢修孔之必要,該檢修孔之安裝方式須能確保天花板氣密。
d.實驗室門板材質必須符合防火要求等級且依防火安全標準設置。
e.前室與公共通道之門、前室與實驗室操作區域之門應採互鎖式設計,並具手動解除互鎖狀態之功能。
f.實驗室觀景窗(視窗)應採用安全玻璃(膠合玻璃)材質,安裝時應緊密密封。
g.地板需使用無縫施工,應採用對氣體和化學物質具耐酸鹼、耐磨、耐壓及止滑功能材料。
h.地板與牆壁間塗層應採曲度導角(cove)型施工。
i.位於阻隔區牆邊外露之管路,其與牆壁間須保留維護保養之空間。
j.所有外露之冷、熱水管路,其外層應包覆絕緣材料,並作防止移動及防震之相關保護措施。
3.實驗室設施
a.必備項目
b.實驗室門上應標示「生物危害標識」及「標準緊急處理程序」。
c.實驗室之氣密門可閉鎖,如設有安全緊急逃生門,應採壓扣式安全門把。
d.實驗室應設傳遞箱及浸泡桶。
e.實驗室內設置之出水設施應為免手動,且具存水彎設計。
f.實驗室內使用之座椅應為不附輪型式。
g.供應實驗室使用之壓縮氣體鋼瓶須放置於實驗室外,且應固定妥善。
h.主要的供水設施控制系統應該設置於實驗室外。
i.所有電路斷電器開關、配電盤和控制器應有適當標示。
j.電路的斷電器應位於實驗室外。
k.實驗室和外界應有適當的聯繫裝置,如免持聽筒式對講機。
l.裝設洗眼設施。
4.實驗室安全措施
a.實驗室人員進出,必須鑰匙或門禁系統實施管制。不使用時,實驗室仍須實施門禁管制。
b.實驗室必須符合消防、安全衛生等相關法規之要求。
c.實驗室應設置對外通訊系統及相關安全監控系統。
d.實驗室內應設置火警警報系統。
e.實驗室應針對火災、地震等天然災害及實驗室生物安全意外事件擬訂實驗室緊急應變計畫。
f.電力系統應設置不斷電系統並聯備用發電機,於緊急狀況時可以維持重要功能。
5.實驗室操作規範
A.進入實驗室前
a.非經實驗室管理人員及(或)實驗室主管之許可,任何人不得進入。
b.新進人員須經適當訓練後,方可進入實驗室操作。
c.實驗室門口應標示生物危害標誌、實驗室管理人員、實驗室主管與緊急聯絡人之姓名、職稱、聯絡方式(如手機)及實驗之病原體種類(備註)等。
d.實驗室操作人員如有身體異常或不適之情形,須向實驗室管 理人員及(或)實驗室主管報告,並暫停進入實驗室工作。
e.人員進出實驗室時,應以書面或其他方式登錄其姓名、進出之日期、時間及事由等。
f.執行具感染風險之操作時,不宜只有1 人進入實驗室工作。僅有1 人進入實驗室時,仍需有另1 人在實驗室外負責監控。
g.實驗室操作人員進入實驗室工作前,應預先列出實驗所需相關物品清單,並逐項核對物品是否齊備。
h.實驗室操作人員於進入實驗室前,應先確認實驗室外部相關監控系統上顯示之實驗室溫、濕度及負壓等數值是否無異常後,方可進入實驗室;如數值異常時,應立即通知實驗室管理人員及(或)實驗室主管。
i.查看實驗室外供應實驗室使用之壓縮氣體鋼瓶,其壓力錶數值是否正常,氣體存量是否足夠使用。
j.實驗用器材應經由傳遞箱傳遞。
k.嚴禁攜帶私人物品進入實驗室內使用。
l.實驗室主管應視操作病原體之屬性,訂定實驗室操作人員穿著防護裝備之標準作業程序,並張貼於人員著裝處(建議採圖文方式呈現)。
B.進入實驗室內
a.先準備吸水性良好之紙巾、酒精棉及消毒液等備用。
b.物安全櫃內勿置放非必要之器材。
c.準備可盛裝棄置吸管類之容器(應預盛適量消毒液)。
d.所有與病原體有關之開放性操作,都應於生物安全櫃中進行,不可在開放的實驗台上進行。實驗操作過程中應盡量減少會產生氣膠之動作,例如更換培養液、上清液移至另一容器、用吸管吸吹液體、使用高速旋轉之機具、於固體培養基表面滴加細菌懸浮液、注射針具抽取感染性液體時推出氣泡等。
e.實驗操作過程中,如手套有任何污染之虞時,應立刻更換外層手套。
f.實驗室內設置之通訊設備(如電話、對講機等)應採免持聽筒方式,如需手持,應先脫去外層手套後方可手持聽筒通話。
g.吸取液體培養液或廢液,要使用具過濾器之管輔助器(pipette aid)。如使用真空馬達吸引潛在性感染液體,必須在近馬達抽氣端加裝消毒液瓶及空氣過濾器,以防污染。
h.操作感染性液體使用的微量吸管尖(micropipette tip)應選用有加裝過濾器者。
h-1.吸管輔助器使用時因不慎受污染,應立即消毒處理並更換過濾膜,以防他人不知情而繼續使用,致受污染。
h-2.用過之吸管、滴管、微量吸管尖等先用消毒液浸泡後,再將其丟入置放在生物安全櫃的垃圾袋。
k.使用過之吸管尖先吸入消毒液後才可退入吸管盤(pipette tray)或丟入置放在生物安全櫃的垃圾袋。
l.使用震盪器(vortex mixer)混合感染性液體時,手執位置應高於試管液面,混合時液體才不會衝到蓋子。
m.實驗操作過程應避免使用易受傷之尖銳物。使用注射針具時,不可以手將使用過之針頭回套。
n.使用注射針具抽取感染性液體後,如需排除氣泡部分,針頭必須朝上,並插入底部填塞棉花之滅菌短試管,以避免產生氣膠。
o.開啟冷凍乾燥菌種(或毒株)安瓿瓶前,需先使用玻璃切割器切割欲折斷部位(手要戴防割材質手套),以酒精棉擦拭後將安瓿瓶插入套管內,外面覆蓋滅菌紗布,再套上塑膠袋,才可折斷安瓿瓶。
p.培養物、組織、體液標本、檢體瓶、培養瓶、試管、離心管及其他盛裝感染性或潛在感染性廢棄物的容器一律放入內舖滅菌專用塑膠袋的耐高溫高壓附蓋(不氣密)防爆桶(或不銹鋼桶),以利處理滅菌。
q.病毒培養瓶整瓶凍結時,解凍前應先套上塑膠袋才可放進 37℃恆溫水槽解凍,以防培養瓶龜裂,瓶內病毒四處流散。
r.病原體標本進出實驗室時,其包裝容器外部必須用消毒液浸泡或擦拭後,始可進行。
s.有關實驗室停電情況,應依擬定緊急應變程序操作。另經評估安全後,操作人員方可再進入。
t.實驗操作中意外遭受感染性物質之潑濺或割傷時,應立即作消毒處理並向實驗室管理人員及(或)實驗室主管報告,及製作紀錄,以利後續追蹤。
u.實驗操作中遇有感染性液體小量溢出或濺灑,應立即以擦手紙、紗布或棉花等沾消毒液覆蓋,經過30 分鐘後再行清理。
v.發生大量感染性液體傾倒意外,或不慎打破盛裝感染性液體之容器時,人員儘速依程序離開實驗室,並報告實驗室管理人員及實驗室主管,由實驗室主管決定處理方式,並作成紀錄以利後續追蹤、監視及評估、進行通報程序。
C.準備離開實驗室
a.實驗紀錄攜出應經由電腦網路、傳真機或PDA等方法傳送,不得以紙本傳送。
b.實驗操作完畢時,需將實驗室現場整理乾淨。使用過之器材,不能用高溫高壓滅菌之可重複使用器材,可用紫外線照射、適當濃度消毒液(如1%維康(Virkon)消毒液)浸泡外,其他器材一律採用高溫高壓滅菌處理。
c.離開實驗室前關閉非必要之電源。
d.登記離開實驗室時間。
e.工作結束或中途需要暫時離開,應依實驗室規定移除個人防護裝備。穿脫程序應製圖張貼於實驗室出入口。
f.離開實驗室前應洗手。
D.生物安全櫃之使用
a.實驗操作前,生物安全櫃至少先開機運轉5 分鐘。
b.實驗操作完畢,生物安全櫃如為ClassII A2 機型,則至少持續運轉5 分鐘,使污染空氣完全清除才可關機。
c.於生物安全櫃內操作時,儘可能減少手部進出動作,不能避免時,進出動作應和緩,以避免破壞操作口之空氣屏障(air barrier)。
d.如有設置紫外線燈,於關機後開紫外線燈,設定照射時間。
e.生物安全櫃內之氣柵(grills)不可以有東西阻擋。
E.個人安全防護
a.實驗室主管應視實際操作病原體之危害屬性,訂定適當個人防護裝備規定。
b.進入實驗室應穿防護衣,戴N95 口罩,穿膠鞋或鞋套,手戴雙層手套,必要時戴護目鏡或面罩,如戴呼吸器則使用過之呼吸器必須經燻蒸消毒處理後,通過濾效及洩漏測試才能再次使用。
c.實驗之病原體如有疫苗可預防,沒有保護抗體之個人,必須事先施打疫苗。
d.實驗室新進工作人員應事先留存血液檢體當檢測基準,並依法保存至人員離職十年後,始可銷毀。必要時定期採取,以利健康管理及追蹤監視。
F.離心機之使用
a.確認離心機蓋具安全設計裝置。
b.檢視離心套管氣密蓋或旋轉盤(rotor)蓋子圓型墊環是否裝妥。
c.確認裝在水平離心頭之套管是否一樣。
d.確認所要用之離心管材質是否合乎所要求的轉速或離心力。
e.一般離心機之離心管檢體量依其離心角度之不同作適度調 整,切記避免過量,以致離心時溢出。
f.超高速離心機之離心管檢體量必須依離心管之規定容量裝放。
g.平衡套管及離心物重量。
h.確認套管與檢體已裝妥並成對角線擺放。
i.啟動離心,使用高轉速離心時應緩慢加速,切忌急速轉到所要之轉速。
j.使用超高速離心機應注意其真空排氣要經HEPA過濾器處理。
k.超高速離心機之旋轉盤,每次使用前應檢視轉盤底部之轉速Disc(黑白相間圓形片)是否貼緊。
l.每次裝放超高速旋轉盤必須確認轉盤與離心機轉軸是否密合。
m.使用超高速旋轉盤必須登錄轉速及使用累計時數。
n.離心機旋轉停止後,取出潛在感染性檢體時,須將離心管移置生物安全櫃中開啟,以防溢出物或氣膠造成感染。
o.超高速離心機之旋轉盤如果受污染,應依該儀器之使用手冊內所述滅菌方式進行,或使用不傷其材質之消毒劑或氧化乙烯(E.O.G)等處理,並留意若使用高壓蒸氣或乾熱滅菌對其材質是否會影響。
G.高溫高壓蒸氣滅菌器
a.欲滅菌之液狀物容器其容量不可超過三分之二以上,且不可緊閉容器口。
b.用過耗材要裝進內舖滅菌專用塑膠袋的耐高溫高壓附蓋(不氣密)防爆桶(或不銹鋼桶),才可送進高溫高壓蒸氣滅菌器內。
c.滅菌物貼滅菌溫度指示帶。
d.隨時緊閉鍋門。
e.物品送入鍋內前先確認另一端之鍋門已關緊。
f.滅菌完成欲打開鍋門時,必先確認內鍋壓力已歸零,才可打開鍋門。
g.應定期或委由代檢機構執行高溫高壓蒸氣滅菌器檢測確效程序。
H.超低溫冷凍櫃
a.實驗室內之超低溫冷凍櫃建議選用小型臥式冷凍櫃,櫃門向上開者,除溫度上升較緩慢,可減少壓縮機運轉時間而節省能源外,且因櫃門向上開,可避免內存之感染性生物材料在開櫃門時掉落地上。
b.存放於冷凍櫃內之感染性生物材料應採用體積小的容器保存,其瓶口應氣密封緊,容器外部應清楚標示內容物名稱、容量、保存日期等,並將該容器放置於檢體保存盒內,且於保存盒外部標示存放者之姓名。
c.保存用容器應選用耐超低溫之材質。
d.儘可能使用塑膠材質保存盒及不銹鋼儲放架存放檢體,以節省儲存空間。
e.定期小心清除冷凍櫃內結冰。
f.超低溫冷凍櫃溫度如果沒有電腦化中央監視系統管理,工作人員應定期自行更換溫度紀錄紙。
g.冷凍櫃內得填塞冰寶(冷媒劑),以防電力異常狀況時,維 持溫度之穩定。
I.冰箱
a.儲放冰箱內之培養基、緩衝液等液體類容器應緊閉瓶口並標示內容物、日期及存放者。
b.冰箱內置一溫度計以便溫度觀測及記錄。
c.每星期或實驗告一階段應整理冰箱內之存放物,廢棄不用者一律高溫高壓滅菌處理。
d.冰箱內禁放具爆炸性之化學品。
J.二氧化碳培養箱
a.培養容器外部應標示培養物、日期及培養者以利識別。
b.定期清洗及更換水盤內蒸餾水。
c.隨時注意二氧化碳桶壓力錶,特別是例假日之前,避免二氧化碳耗盡影響培養物之生長。
e.有培養物滲漏、污染,應立即清除消毒。
K.恆溫水槽
a.水位不可低於電熱管,注意隨時添加水量。
b.定期清洗恆溫水槽。
c.下班之前,關閉不用的水槽加熱器。
d.有感染物污染時,將水溫調高到75℃,持續加溫一小時,待溫度降下後加適當濃度消毒液,如1%維康消毒液消毒,清洗,更換蒸餾水。
L.紫外線燈
a.定期擦拭紫外線燈管。
b.定期檢測燈管紫外線強度,必要時更換燈管確保殺菌效果。
c.工作中不可開紫外線燈。
d.組織研磨機(Homogenizer or Tissue Blender)
e.選用刀片機組能氣密緊閉。
f.組織研磨必須在生物安全櫃內,操作開始時,先用低速再用高速。研磨時應在冷溫中進行(浸在冰水內)研磨後,在冰水內靜置至少15 分鐘,待產生之氣膠沉降後才打開,可減少氣膠污染。
g.用過的刀片機組浸在不傷刀具之適當濃度消毒液,如1%維康消毒液,隨即高溫高壓滅菌消毒。
h.拆卸刀片清洗、烘乾、包裝滅菌後備用。
M.實驗室之清潔、消毒
a.定期整理清潔。
b.實驗室應使用不掉纖維之抹布,先浸泡消毒液擦拭後,再用清水擦拭乾淨。
c.地板以無塵室專用之滾輪粘紙拖拭。
d.實驗結束,告一階段或轉換實驗不同病原體之前,應進行適當之燻蒸或消毒作業。
e.儀器設備需要維修時,應先徹底做好適當消毒措施,但生物安全櫃之維修則應先進行燻蒸消毒,以維護工作人員健康權益。
f.更換空調HEPA 過濾器之前先作燻蒸消毒處理。
g.實驗室發生嚴重污染時需作燻蒸消毒。
h.病原體之包裝及運送有關感染性物質之包裝及運送,應依照疾病管制局出版
之「防疫檢體採檢手冊」規定辦理。另可參考WHO「感染性物質運輸規則指引(Guidance on regulations for theTransport of Infectious Substances)」及國際航空運輸協會(International Air Transport Association, IATA)相關指引。







